Cada año, miles de dispositivos médicos se envían a la Administración de Alimentos y Medicamentos (FDA) para su aprobación, pero no todos logran los requisitos. Sin embargo, en estos últimos años se ha visto un aumento en la cantidad de dispositivos aprobados por la FDA.
Luego de presentar pruebas de que los dispositivos son seguros y efectivos, se aprueban para entrar al mercado. Hasta julio de 2022 se han aprobado 18 dispositivos médicos nuevos. Conoce los seis nuevos dispositivos aprobados por la FDA enfocados en mejorar las operaciones y tratamientos del corazón.
1) Organ Care System (OCS™) Heart System
Compañía: TransMedics, Inc.
Fecha de aprobación: 27 de abril de 2022
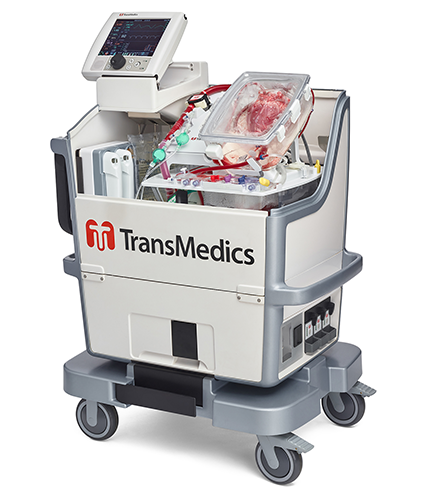
El TransMedics Organ Care System (OCS) Heart System se diseñó para preservar los corazones donados antes de ser trasplantados. El equipo incluye un espacio encerrado que calienta el corazón donado y le proporciona el oxígeno y los nutrientes necesarios para su preservación.
2) Thoraflex Hybrid
Compañía: Terumo Aortic (Vascutek Limited)
Fecha de aprobación: abril 19 de 2022
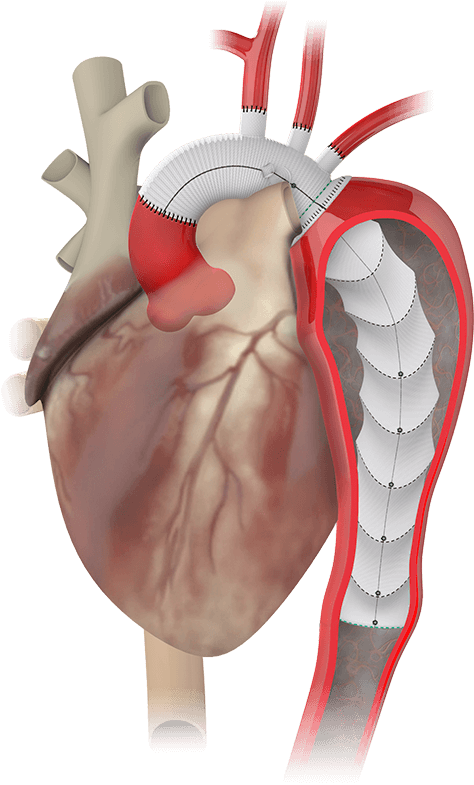
El dispositivo Thoraflex Hybrid se diseñó para reparar secciones debilitadas de aneurisma o desgarros en la disección del arco aórtico, detrás del corazón. El sistema incluye un injerto de poliéster que refuerza la sección débil del vaso sanguíneo, una sección que permite mantener la arteria abierta, y un catéter utilizado para colocar el dispositivo. Se utiliza durante operaciones a corazón abierto para reparar o reemplazar las secciones dañadas o enfermas del arco aórtico y la parte que fluye hacia el corazón.
3) Aveir™ Leadless Pacemaker System
Compañía: Abbott Medical
Fecha de aprobación: 31 de marzo de 2022

El dispositivo de marcapasos inalámbrico corrige los ritmos cardíacos lentos o irregulares a través de pulsos eléctricos que permiten que el corazón lata de forma regular. El sistema incluye el marcapasos inalámbrico junto al catéter de entrega y un módulo de enlace. Los doctores lo implantan al hacer una pequeña incisión en la pierna del paciente utilizando el catéter para unirlo al ventrículo derecho del corazón. Luego de su implantación, se añaden electrodos del módulo en la piel del paciente a los que el doctor se conecta de forma inalámbrica y ajusta el marcapasos a las necesidades del paciente.
4) CardioMEMS HF System
Compañía: St. Jude Medical / Abbott
Fecha de aprobación: 18 de febrero de 2022
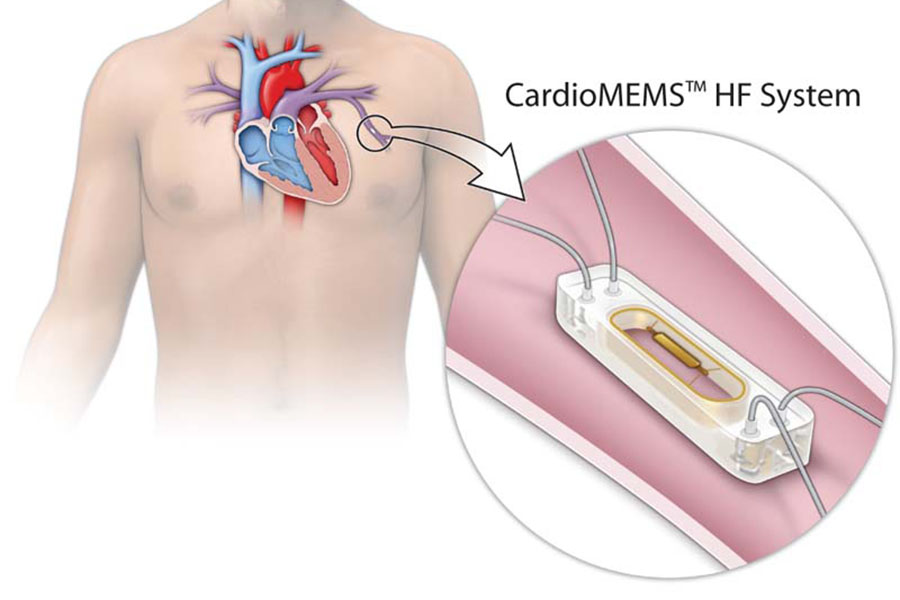
El sistema inalámbrico de CardioMEMS HF permite medir y monitorear la presión de las arterias pulmonares y el ritmo cardíaco de pacientes con insuficiencia cardíaca. Se trata de un sensor implantable que se une a la arteria pulmonar con un tubo flexible en un procedimiento poco invasivo al corazón. El sensor permite monitorear la presión de la sangre que fluye por la arteria pulmonar y permite tomar lecturas diarias de la presión. En miras de disminuir las hospitalizaciones por fallas del corazón, la nueva aprobación del producto ahora incluye a los pacientes con insuficiencia cardiaca menos severa.
5) ENROUTE Transcarotid Stent System
Compañía: Silk Road Medical, Inc.
Fecha de aprobación: 28 de abril de 2022
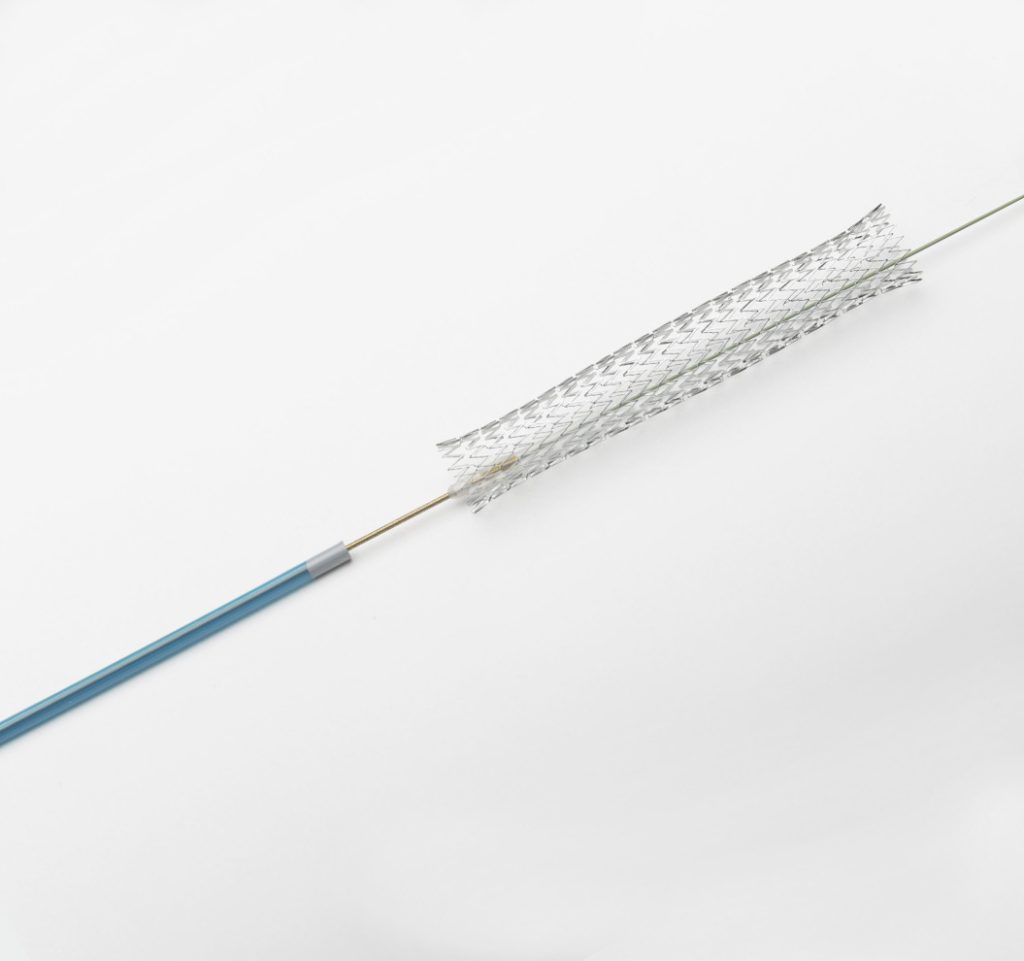
El implante autoexpandible de ENROUTE Transcarotid Stent System se utiliza durante cirugías para reabrir partes estrechas de las arterias carótidas, que llevan sangre al cerebro. El dispositivo, ya aprobado anteriormente en pacientes de alto riesgo, ahora incluye a pacientes con riesgo a nivel regular. El aparato se utiliza en las cirugías junto con el ENROUTE NPS que evita que el flujo sanguíneo se escape. Así, el implante mantiene abiertas las arterias carótidas que tienen obstrucciones para evitar posibles accidentes cerebrovasculares.
6) Eversense E3 Continuous Glucose Monitoring System
Compañía: Senseionics, Inc.
Fecha de aprobación: 10 de febrero de 2022

El Eversense E3 Continuous Glucose Monitoring System trata de un sensor implantable que lee la glucosa a tiempo real cada cinco minutos para las personas con diabetes. El sistema incluye una aplicación de teléfono que presenta los resultados y envía alertas a través de un transmisor inalámbrico. Los doctores lo implantan debajo de la piel para monitorear cuánta azúcar se presenta en el flujo sanguíneo. Las personas lo pueden tener hasta 180 días debajo de la piel, y deben ser de 18 años o mayores. Para calibrar el dispositivo, se deben hacer pruebas de sangre en el dedo una o dos veces al día con un medidor de glucosa.
Presione aquí para ver la segunda parte de los dispositivos médicos aprobados por la FDA.